全文转载自“iNature”公众微信号
神经元中含有大量针对神经元增强子的单链DNA断裂(single-strand breaks, SSBs),但这种内源性损伤的来源尚不清楚。
2022年12月1日,美国国立卫生研究院(NIH)的André Nussenzweig及吴薇共同通讯在Science杂志在线发表题为“Active DNA demethylation promotes cell fate specification and the DNA damage response”的研究论文,André Nussenzweig课题组的博士后王东鹏,吴薇(现为中科院分子细胞科学卓越创新中心研究员)和Elsa Callen为该论文的共同第一作者。
该研究以有丝分裂后的神经元和巨噬细胞为研究体系,发现DNA主动去甲基化对于增强子激活是必要的,并且解释了神经元和巨噬细胞增强子上DNA单链损伤的来源以及阐述其中的机制。

在哺乳动物基因组中,胞嘧啶的第5位碳原子的甲基化(5-甲基胞嘧啶,5-methylcytosine或5mC)是丰度最高的DNA修饰类型,也被称为“第5种碱基”。5mC由DNA甲基化酶DNMTs催化,主要富集在CpG岛。虽然5mC的分布具有组织特异性,但70-80%的CpG岛都具有5mC修饰。5-羟甲基胞嘧啶(5-hydroxymethylcytosine或5hmC),也被称为第6碱基,由TET1酶氧化5mC而来。5hmC的进一步氧化产生5-甲酰基胞嘧啶(5fC)和5-羧基胞嘧啶(5caC)。TET在有丝分裂后的神经元中高度活跃,在其他体细胞类型中程度较低。一个未解决的问题是,复制无关的去甲基化在多大程度上有助于细胞分化和功能。
DNA修复缺陷导致癌症易感性和神经疾病。尽管所有类型的细胞都会导致DNA损伤和突变,但神经元对单链断裂(SSB)修复缺陷异常脆弱。SSB由XRCC1和PARP(poly-ADP ribose polymerase)检测,它们招募参与DNA末端修饰的因子(polynucleotide kinase 3′-phosphatase, PNKP ;aprataxin, APTX),DNA间隙填充(POLβ, DNA聚合酶β家族)和连接(DNA连接酶1或3)。这些蛋白质是大多数SSB修复事件所必需的,通常包括“短补丁”反应,其中只有一个缺失的核苷酸被替换。更罕见的是,使用长补丁子通路,在结扎前使用扩展的DNA合成。然而,长补丁SSB修复不能完全补偿短补丁SSB修复的损失,这一点可以从神经疾病与短补丁修复所需基因突变的关联中得到证明,如XRCC1、APTX和PNKP。
最近,该团队与合作者证明,神经元中SSB的高活性长补丁合成相关修复(synthesis-associated repair, SAR)可以通过加入5-乙基-2 ' -脱氧尿苷( 5-ethynyl-2′-deoxyuridine, EdU) (SAR-seq)检测到。DNA修复合成和SSBs定位于神经元增强子,对应2%的基因组。然而,为什么神经元将修复机制集中到这些热点是一个未解决的问题。此外,内源性SSB的来源及其生理相关性尚不清楚。
在这项研究中,研究人员使用两种有丝分裂后谱系说明系统——诱导的多能干细胞来源的神经元和转分化的巨噬细胞——研究人员发现胸腺苷DNA糖基化酶(thymidine DNA glycosylase, TDG)驱动的甲基胞嘧啶被10-11易位酶(translocation enzymes, TET)氧化的切除是SSBs的来源之一。
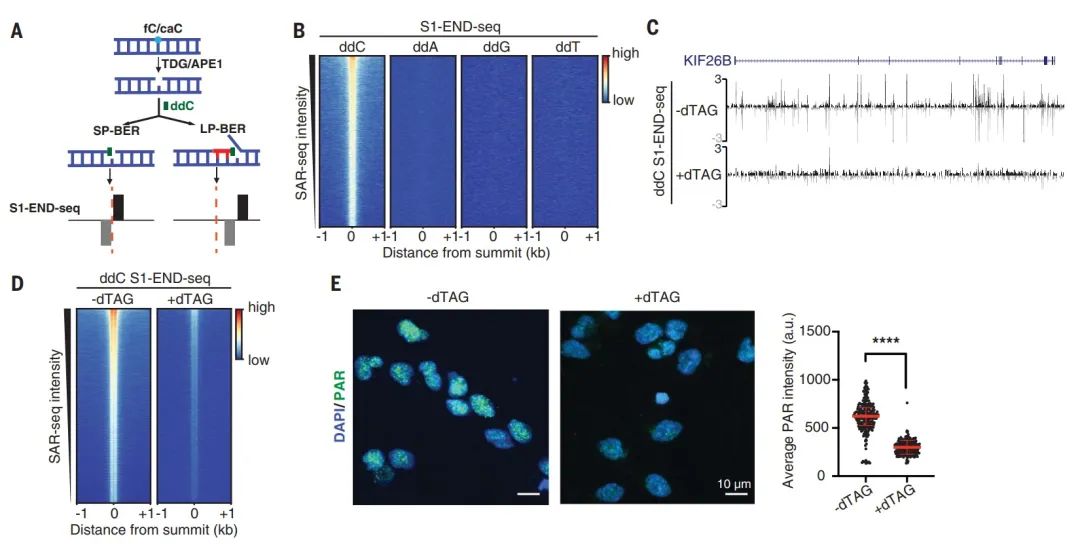
图1. 神经元增强子的单链断裂依赖于TDG(图源自Science )
进一步研究表明,尽管巨噬细胞分化倾向于短斑块基切除修复来填补单核苷酸间隙,但神经元也经常使用长斑块子通路。通过使用抗肿瘤胞嘧啶类似物破坏这一间隙填充过程会触发DNA损伤反应和神经元细胞死亡,这依赖于TDG。因此,TET介导的活性DNA去甲基化促进内源性DNA损伤,这一过程通常保护细胞的身份,但也可能在抗癌治疗后引发神经毒性。
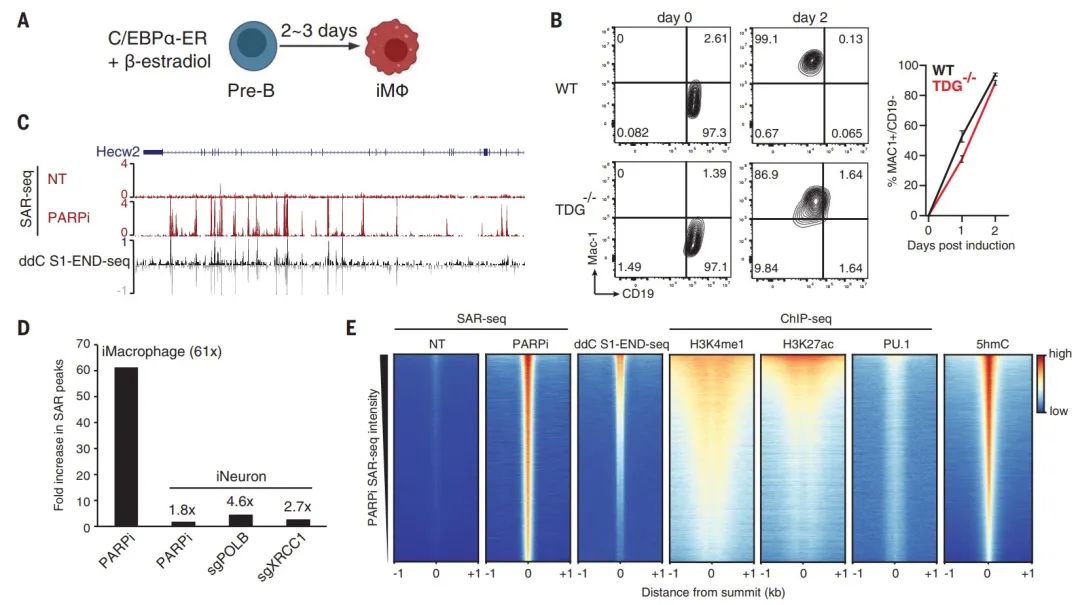
图2. 巨噬细胞增强子上TDG依赖的SSBs(图源自Science )
结合这项发现,确定TDG抑制剂或触发DNA损伤反应的其他通路成分的抑制剂是否有希望缓解与抗癌药物治疗相关的一些神经系统并发症将是一件有趣的事情。
原文链接:
https://www.science.org/doi/10.1126/science.add9838
